甲酸
|
[拼音]:jiasuan [外文]:formic acid
甲酸的性质与其他羧酸有所不同。甲酸为有刺激臭味的无色液体,有很强的腐蚀性,能刺激皮肤起泡。甲酸的熔点8.4℃,沸点100.7℃,相对密度1.220(20/4℃);能与水、醇、醚混溶。甲酸的羧基直接与氢原子相连,既可看成是一种羧酸,又可看成是一种羟基醛,它同时具有羧酸和醛(见醛和酮)的某些性质。例如,甲酸具有酸性,而且比同系列中其他酸的酸性都强,能生成盐和酯,体现了羧基的性质;另一方面,它与醛类似,具有还原性,例如能使硝酸银的氨水溶液(称为土伦试剂)还原成金属银,能使高锰酸钾褪色,这些反应也可作为检验甲酸的方法。甲酸不很稳定,较易脱羧,加热至160℃即分解成二氧化碳和氢气。甲酸与浓硫酸共热,则分解成一氧化碳和水。实验室里常用此法来制备少量高纯度的一氧化碳。 甲酸的工业制法是用粉状的氢氧化钠与一氧化碳在120~130℃和6~8大气压下反应,首先生成甲酸钠,然后将干燥的甲酸钠加到浓硫酸和甲酸的混合液中,再经减压蒸馏,即得无水甲酸。实验室制法是将草酸和甘油于110℃共热,先生成草酸的一元甘油酯,再失去二氧化碳而生成甲酸的一元甘油酯,最后水解成甘油和甲酸,经蒸馏得最高含量为77%的甲酸水溶液,即甲酸与水的共沸混合物。 甲酸广泛用于染料和制革工业,也是常用的消毒剂和防腐剂,还可做橡胶胶浆的凝结剂,及用于制药和有机合成。甲酸铝是优良的防水剂。甲酸甲酯和乙酯是熏蒸消毒剂,甲酸丁酯和戊酯是清漆的溶剂。 |

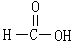 又称蚁酸,因最早由蒸馏赤蚁获得,故得名。甲酸是最简单的羧酸,分子式HCOOH。甲酸在自然界分布很广,并常以游离状态存在,如在赤蚁、蜂、毛虫的分泌物中;某些植物如荨麻、蝎子草、松针和一些果实(如绿葡萄),以及人体的肌肉、皮肤、血液和排泄物中都含有甲酸。
又称蚁酸,因最早由蒸馏赤蚁获得,故得名。甲酸是最简单的羧酸,分子式HCOOH。甲酸在自然界分布很广,并常以游离状态存在,如在赤蚁、蜂、毛虫的分泌物中;某些植物如荨麻、蝎子草、松针和一些果实(如绿葡萄),以及人体的肌肉、皮肤、血液和排泄物中都含有甲酸。