计时电流法
|
[拼音]:jishi dianliufa [外文]:chronoamperometry 一种研究电极过程动力学的电化学分析法和技术。在电解池上突然施加一个恒电位,足够使溶液中某种电活性物质(或称去极剂)发生氧化或还原反应,记录电流与时间的变化,得到电流-时间曲线,故称计时电流法(见图)。 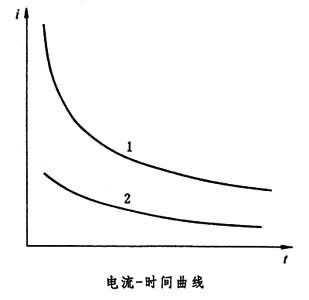
1922年J.海洛夫斯基在发明极谱法的同时重新强调了计时电流法,它可以采用极谱仪的基本线路。但要连接快速记录仪或示波器,不用滴汞电极,而用静止的悬汞、汞池或铂、金、石墨等电极,也不搅动溶液。在大量惰性电解质存在下,传质过程主要是扩散。 1902年美国F.G.科特雷耳根据扩散定律和拉普拉斯变换,对一个平面电极上的线性扩散作了数学推导,得到科特雷耳方程: 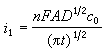
式中i1为极限电流;F为法拉第常数;n为电极反应的电子转移数;A为电极面积;c0为活性物在溶液中的初始摩尔浓度;D为活性物的扩散系数;t为电解时间。 当时间趋向于无穷大,电流就趋近于零,这是因为电极表面活性物的浓度由于电解而逐渐减小的结果。利用i1或i1t1/2与c0成正比的关系,可用于定量分析,但由于此法不如极谱法准确和重现性好,所以实际上很少应用。因为 科特雷耳方程适用于扩散过程(图中曲线1),如果电极反应不可逆或伴随化学反应时,则动力电流ik随时间的变化见图中曲线2,它受反应速率常数的控制。 计时电流法常用于电化学研究,即电子转移动力学研究。近年来还有采用两次电位突跃的方法,称为双电位阶的计时电流法。第一次突然加一电位,使发生电极反应,经很短时间的电解,又跃回到原来的电位或另一电位处,此时原先的电极反应产物又转变为它的原始状态,从而可以在i-t曲线上更好地观察动力学的反应过程;并从科特雷耳方程出发,考虑反应速率,进行数学推导和作图,求出反应速率常数。 |

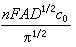 是一个常数,所以i1t1/2对t作图得一不随t变化的直线。
是一个常数,所以i1t1/2对t作图得一不随t变化的直线。


















